Аминокислоты с металлами реакция. Химические свойства аминокислот. Образование солей с щелочами и карбонатами щелочных металлов
1.Аминокислоты проявляют амфотерные свойства и кислот и аминов, а также специфические свойства, обусловленные совместным присутствием указанных групп. В водных растворах АМК существуют в виде внутренних солей (биполярных ионов). Водные растворы моноаминомонокарбоновых кислот на лакмус нейтральны, т.к. в их молекулах содержится равное число -NН 2 - и -СООН групп. Эти группы взаимодействуют между собой с образованием внутренних солей:
Такая молекула имеет в двух местах противоположные заряды: положительный NН 3 + и отрицательный на карбоксиле –СОО - . В связи с этим внутренняя соль АМК имеет название биполярного иона или Цвиттер–иона (Zwitter – гибрид).
Биполярный ион в кислой среде ведет себя как катион, так как подавляется диссоциация карбоксильной группы; в щелочной среде – как анион. Существуют значения рН специфические для каждой аминокислоты, в которой количество анионных форм в растворе равно количеству катионных форм. Значение рН при котором общий заряд молекулы АМК равен 0, называется изоэлектрической точкой АМК (pI АК).
Водные растворы моноаминодикарбоновых кислот обладают кислой реакцией среды:
HООС-СH 2 -СH-СOOH « - OOC-CH 2 -CH–COO - + H +
Изоэлектрическая точка моноаминодикарбоновых кислот находится в кислой среде и такие АМК называют кислыми.
Диаминомонокарбоновые кислоты обладают в водных растворах основными свойствами (участие воды в процессе диссоциации показывать обязательно):
NH 2 -(CH 2) 4 -CH-COOH + H 2 O « NH 3 + -(CH 2) 4 -CН–COO - + OH -
Изоэлектрическая точка диаминомонокарбоновых кислот находится в при рН>7 и такие АМК называют основными.
Являясь биполярными ионами, аминокислоты проявляют амфотерные свойства: они способны образовывать соли как с кислотами, так и с основаниями:
Взаимодействие с соляной кислотой HCl приводит к образованию соли:
R-CH-COOH + HCl ® R-CH-COOH
NH 2 NH 3 + Сl -
Взаимодействие с основанием приводит к образованию соли:
R-CH(NH 2)-COOH + NaOH ® R-CH(NH 2)-COONa + H 2 O
2. Образование комплексов с металлами – хелатный комплекс. Строение медной соли гликокола (глицина) можно изобразить следующей формулой:

Почти вся имеющаяся в организме человека медь (100 мг) связана с белками (аминокислотами) в виде этих устойчивых клешневидных соединений.
3. Подобно другим кислотам аминокислоты образуют сложные эфиры, галоген ангидриды, амиды.
4. Реакции декарбоксилирования протекают в организме при участии специальных ферментов декарбоксилаз: получающиеся при этом амины (триптамин, гистамин, серотинин) называются биогенными аминами и являются регуляторами ряда физиологических функций человеческого организма.
5. Взаимодействие с формальдегидом (альдегидами)
R-CH-COOH + H 2 C=О ® R-CH-COOH
Формальдегид связывает NН 2 – группу, -СООН группа остается свободной и может быть оттитрована щелочью. Поэтому данная реакция используется для количественного определения аминокислот (метод Сёренсена).
6. Взаимодействие с азотистой кислотой приводит к образованию гидроксикислот и выделению азота. По объему выделившегося азота N 2 определяют его количественное содержание в исследуемом объекте. Эта реакция применяется для количественного определения аминокислот (метод Ван–Слайка):
R-CH-COOH + HNO 2 ® R-CH-COOH + N 2 + H 2 O
Это один из способов дезаминирования АМК вне организма
7. Ацилирование аминокислот. Аминогруппу АМК можно ацилировать хлорангидридами и ангидридами кислот уже при комнатной температуре.
Продуктом записанной реакции является ацетил-α-аминопропионовая кислота.
Ацильные производные АМК широко используются при изучении последовательности их в белках и в синтезе пептидов (защита аминогруппы).
8.Специфические свойства, реакции, связанные с наличием и взаимным влиянием амино- и карбоксильной групп - образование пептидов. Общим свойством a-АМК является процесс поликонденсации , приводящий к образованию пептидов. В результате этой реакции формируются амидные связи по месту взаимодействию карбоксильной группы одной АМК и аминогруппы другой АМК. Другими словами, пептиды – это амиды, образующиеся в результате взаимодействия аминогрупп и карбоксилов аминокислот. Амидная связь в таких соединениях называется пептидной связью (разобрать строение пептидной группы и пептидной связи: трехцентровая р,p-сопряженная система)
В зависимости от числа аминокислотных остатков в молекуле различают ди-, три-, тетрапептиды и т.д. вплоть до полипептидов (до 100 остатков АМК). Олигопептиды содержат от 2 до 10 остатков АМК, белки - более100 остатков АМК.В общем виде полипептидную цепь можно представить схемой:
H 2 N-CH-CO-NH-CH-CO-NH-CH-CO-... -NH-CH-COOH
Где R 1 , R 2 , … R n – радикалы аминокислот.
Понятие о белках.
Наиболее важными биополимерами аминокислот являются белки – протеины. В организме человека насчитывается около 5млн. различных белков, которые входят в состав кожи, мышц, крови и других тканей. Белки (протеины) получили свое название от греческого слова «protos» - первый, важнейший. Белки выполняют ряд важнейших функций в организме: 1. Строительная функция; 2. Транспортная функция; 3. Защитная функция; 4. Каталитическая функция; 5. Гормональная функция; 6. Питательная функция.
Все природные белки образуются из мономеров аминокислот. При гидролизе белков образуется смесь АМК. Этих АМК – 20.
4. Иллюстративный материал: презентация
5. Литература:
Основная литература:
1. Биоорганическая химия: учебник. Тюкавкина Н.А., Бауков Ю.И. 2014г.
- Сейтембетов Т.С. Химия: учебник - Алматы: ТОО"ЭВЕРО", 2010. - 284 с
- Болысбекова С. М. Химия биогенных элементов: учебное пособие - Семей, 2012. - 219 с. : ил
- Веренцова Л.Г. Неорганическая,физическая и коллоидная химия: учебное пособие - Алматы: Эверо, 2009. - 214 с. : ил.
- Физическая и коллоидная химия /Под ред.А.П.Беляева.- М.: ГЭОТАР МЕДиа, 2008
- Веренцева Л.Г. Неорганическая, физическая и коллоидная химия,(проверочные тесты) 2009
Дополнительная литература:
- Равич-Щербо М.И., Новиков В.В. Физическая и коллоидная химия. М. 2003.
2. Слесарев В.И. Химия. Основы химии живого. С-Пб.: Химиздат, 2001
3. Ершов Ю.А. Общая химия. Биофизическая химия. Химия биогенных элементов. М.: ВШ, 2003.
4. Асанбаева Р.Д., Илиясова М.И. Теоретические основы строения и реакционной способности биологически важных органических соединений. Алматы, 2003.
- Руководство к лабораторным занятиям по биоорганической химии под ред. Н.А. Тюкавкиной. М., Дрофа,2003.
- Глинка Н.Л. Общая химия. М.,2003.
- Пономарев В.Д. Аналитическая химия ч.1,2 2003
6. Контрольные вопросы (обратная связь):
1. Что преопределяет структуру полипептидной цепи в целом?
2. К чему приводит денатурация белка?
3. Что называют изоэлектрической точкой?
4. Какие аминокислоты называются незаменимыми?
5. Каким же образом белки образуются в нашем организме?
Похожая информация.
Аминокислоты (АК) - органические молекулы, которые состоят из основной аминогруппы (-NH 2), кислотной карбоксильной группы (-СООН), и органической R радикала (или боковой цепи), которая является уникальной для каждой АК
Структура аминокислот
Функции аминокислот в организме
Примеры биологических свойств АК. Хотя в природе встречается более 200 различных АК только около одной десятой из них включаются в белки, другие выполняют иные биологические функции:
- Они строительные блоки белков и пептидов
- Предшественники многих биологически важных молекул, производных АК. Например, тирозин является предшественником гормона тироксина и пигмента кожи меланина, тирозин также предшественник соединения ДОФА (диокси-фенилаланина). Это нейромедиатор передачи импульсов в нервной системе. Триптофан является предшественником витамина В3 - никотиновой кислоты
- Источники серы - серосодержащие АК.
- АК участвуют во многих метаболических путях, таких как глюконеогенез - синтез глюкозы в организме, синтез жирных кислот и др.
В зависимости от положения аминогруппы относительно карбоксильной группы АК могут быть альфа, α-, бета, β- и гамма,γ.
|
Альфа - аминогруппа присоединена к углероду, примыкающему к карбоксильной группе:
|
Бета - аминогруппа находятся на 2-м углероде от карбоксильной группы
|
Гамма - аминогруппа на 3-м углерое от карбоксильной группы
|
В состав белков в ходят только альфа-АК
Общие свойства альфа-АК белков
1 - Оптическая активность - свойство аминокислот
Все АК, за исключекнием глицина, проявляют оптическую активность, т.к. содержат по крайней мере один асимметричный атом углерода (хиральный атом).
Что представляет собой асимметричный атом углерода? Это атом углерода, к которому присоединены четыре различных химических заместителя. Почему глицина не проявляет оптическую активность? В его радикале только три разных заместителя, т.е. альфа-углерод не асимметричный.
Что означает оптическая активности? Это означает, что АК в растворе может присутствовать в двух изомерах. Правовращающий изомер (+), который обладает способностью вращать плоскость поляризацованного света вправо. Левовращающий изомер (-), который обладает способностью вращать плоскость поляризации света влево. Оба изомера могут вращать плоскость поляризации света на одну ту же величину, но в противоположном направлении.
2 - Кислотно-основные свойства
В результате их способности к ионизации можно записать следующее равновесие этой реакции:
R-СООН<-------> R-C00 - + H +
R- NH 2 <--------->R-NH 3 +
Поскольку эти реакции обратимы это означает, что они могут действовать как кислоты (прямая реакция) или как основания (обратная реакция), что объясняет амфотерные свойства аминокислот.
Цвиттер ион - свойство АК
Все нейтральные аминокислоты при физиологическом значении рН (около 7,4) присутствуют как цвиттерионы - карбоксильная группа непротонированная и аминогруппа протонированная (рис.2). В растворах более основных, чем изоэлектрическая точка аминокислоты (ИЭТ), аминогруппа -NH3 + в АК жертвует протон. В растворе более кислом, чем ИЭТ АК, карбоксильная группа -СОО - в АК принимает протон. Таким образом, АК иногда ведет себя как кислота, в другие время как основание в зависимости от рН раствора.
Полярность как общее свойство аминокислот
При физиологическом рН АК присутствуют как цвиттер ионы.Положительный заряд несет альфа -аминогруппа, а отрицательный карбоновая. Таким образом, создаётся два противоволожных заряда с обеих концов молекулы АК, молекула имеет полярные свойства.
Наличие изоэлектрической точки (ИЭТ) - свойство амингокислот
Значение рН, при котором чистый электрический заряд аминокислоты равен нулю, и, следовательно, она не может перемещаться в электрическом поле называется ИЭТ.
Способность поглощать в ультрафиолете - свойство ароматических аминокислот
Фенилаланин, гистидин, тирозин и триптофан поглощают при 280 нм. На рис. оторажены значения молярного коэффициента экстинкции (ε) этих АК. В видимой части спектра аминокислоты не поглощают, следовательно, они бесцветны.
АК могут присутствовать в двух вариантах изомеров: L-изомера и D- изомера, которые являются зеркальными отражениями, и отличаются расположением химических групп вокруг атома α-углерода.
изомера, которые являются зеркальными отражениями, и отличаются расположением химических групп вокруг атома α-углерода.
Все аминокислоты в белках в L-конфигурации, L-аминокиcлоты.
Физические свойства аминокислоты
Аминокислоты в основном водорастворимые, что объясняется их полярностью и наличием заряженных групп. Они растворимы в полярных и не растворяется в неполярных растворителях.
АК имеют высокую температуру плавления, что отражает наличие сильных связей, поддерживающих их кристаллическую решетку.
Общие свойства АК является общим для всех АК и во многих случаях определяются альфа-аминогруппой и альфа- карбоксильной группой. АК обладают и специфическими свойствами, которые диктуются уникальной боковой цепью.
Аминокислоты — это органические амфотерные соединения. Они содержат в составе молекулы две функциональные группы противоположного характера: аминогруппу с основными свойствами и карбоксильную группу с кислотными свойствами. Аминокислоты реагируют как с кислотами, так и с основаниями:
Н 2 N -СН 2 -СООН + HCl → Сl [Н 3 N-СН 2 -СООН],
Н 2 N -СН 2 -СООН + NaOH → H 2 N-CH 2 -COONa + Н 2 О.
При растворении аминокислот в воде карбоксильная группа отщепляет ион водорода, который может присоединиться к аминогруппе. При этом образуется внутренняя соль, молекула которой представляет собой биполярный ион:
H 2 N-CH 2 -СООН + Н 3 N -СН 2 -СОO — .
Кислотно-основные превращения аминокислот в различных средах можно изобразить следующей общей схемой:
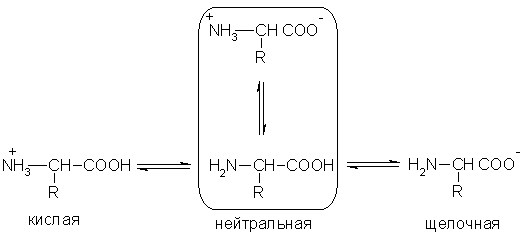
Водные растворы аминокислот имеют нейтральную, щелочную или кислую среду в зависимости от количества функциональных групп. Так, глутаминовая кислота образует кислый раствор (две группы -СООН, одна -NH 2), лизин — щелочной (одна группа -СООН, две -NH 2).
Подобно первичным аминам, аминокислоты реагируют с азотистой кислотой, при этом аминогруппа превращается в гидроксогруппу, а аминокислота - в гидроксикислоту:
H 2 N-CH(R)-COOH + HNO 2 → HO-CH(R)-COOH + N 2 + H 2 O
Измерение объема выделившегося азота позволяет определить количество аминокислоты (метод Ван-Слайка ).
Аминокислоты могут реагировать со спиртами в присутствии газообразного хлороводорода, превращаясь в сложный эфир (точнее, в хлороводородную соль эфира):
H 2 N-CH(R)-COOH + R’OH H 2 N-CH(R)-COOR’ + Н 2 О.
Сложные эфиры аминокислот не имеют биполярной структуры и являются летучими соединениями.
Важнейшее свойство аминокислот - их способность к конденсации с образованием пептидов.
Качественные реакции .
1) Все аминокислоты окисляются нингидрином

с образованием продуктов, окрашенных в сине-фиолетовый цвет. Иминокислота пролин дает с нингидрином желтое окрашивание. Эта реакция может быть использована для количественного определения аминокислот спектрофотометрическим методом.
2) При нагревании ароматических аминокислот с концентрированной азотной кислотой происходит нитрование бензольного кольца и образуются соединения, окрашенные в желтый цвет. Эта реакция называется ксантопротеиновой (от греч. ксантос - желтый).
Аминокислоты - главный строительный материал любого живого организма. По своей природе они являются первичными азотистыми веществами растений, которые синтезируются из почвы. Строение и и аминокислот зависят от их состава.
Структура аминокислоты
Каждая ее молекула имеет карбоксильные и аминные группы, которые соединены с радикалом. Если аминокислота содержит 1 карбоксильную и 1 амино-группу, строение ее можно обозначить формулой, представленной ниже.

Аминокислоты, которые имеют 1 кислотную и 1 щелочную группу, называют моноаминомонокарбоновыми. В организмах также синтезируются и функции которых обусловливают 2 карбоксильных группы или 2 аминных группы. Аминокислоты, содержащие 2 карбоксильные и 1 аминную группы, называют моноаминодикарбоновыми, а имеющие 2 аминные и 1 карбоксильную - диаминомонокарбоновыми.
Также они различны по строению органического радикала R. У каждой из них имеется свое наименование и структура. Отсюда и различные функции аминокислот. Именно наличие кислотной и щелочной групп обеспечивает ее высокую реактивность. Эти группы соединяют аминокислоты и образуют полимер - белок. Белки еще именуются полипептидами из-за своего строения.
Аминокислоты как строительный материал
Молекула белка - это цепочка из десятков или сотен аминокислот. Белки отличаются по составу, количеству и порядку расположения аминокислот, ведь число сочетаний из 20 составляющих практически бесконечно. Одни из них имеют весь состав незаменимых аминокислот, иные обходятся без одной или нескольких. Отдельные аминокислоты, структура, функции которых подобны белкам человеческого тела, не применяются в качестве пищевых, так как малорастворимы и не расщепляются ЖКТ. К таким принадлежат белки ногтей, волос, шерсти или перьев.
Функции аминокислот трудно переоценить. Эти вещества выступают главной пищей в рационе людей. Какую функцию выполняют аминокислоты? Они увеличивают рост мышечной массы, помогают укреплению суставов и связок, восстанавливают поврежденные ткани организма и участвуют во всех процессах, происходящих в теле человека.

Незаменимые аминокислоты
Только из добавок или пищевых продуктов можно получить Функции в процессе формирования здоровых суставов, крепких мышц, красивых волос очень значимы. К таким аминокислотам относятся:
- фенилаланин;
- лизин;
- треонин;
- метионин;
- валин;
- лейцин;
- триптофан;
- гистидин;
- изолейцин.
Функции аминокислот незаменимых
Эти кирпичики выполняют важнейшие функции в работе каждой клетки человеческого организма. Они незаметны, пока поступают в организм в достаточном количестве, но их недостаток существенно ухудшает работу всего организма.
- Валин возобновляет мышцы, служит отличным источником энергии.
- Гистидин улучшает состав крови, способствует восстановлению и росту мышц, улучшает работу суставов.
- Изолейцин помогает выработке гемоглобина. Контролирует количество сахара в крови, повышает энергичность человека, выносливость.
- Лейцин укрепляет иммунитет, следит за уровнем сахара и лейкоцитов в крови. Если уровень лейкоцитов завышен: он их понижает и подключает резервы организма для ликвидации воспаления.
- Лизин помогает усвоению кальция, что формирует и укрепляет кости. Помогает выработке коллагена, улучшает структуру волос. Для мужчин это отличный анаболик, так как он наращивает мышцы и увеличивает мужскую силу.
- Метионин нормализует работу пищеварительной системы и печени. Участвует в расщеплении жиров, убирает токсикоз у беременных, благотворно влияет на волосы.
- Треонин улучшает работу ЖКТ. Повышает иммунитет, участвует в создании эластина и коллагена. Треонин препятствует отложению жира в печени.
- Триптофан отвечает за эмоции человека. Вырабатывает серотонин - гормон счастья, тем самым нормализует сон, поднимает настроение. Укрощает аппетит, благотворительно влияет на сердечную мышцу и артерии.
- Фенилаланин служит передатчиком сигналов от нервных клеток в мозг головы. Улучшает настроение, подавляет нездоровый аппетит, улучшает память, повышает восприимчивость, снижает боль.
Дефицит незаменимых аминокислот приводит к остановке роста, нарушению обмена веществ, снижению мышечной массы.

Заменимые аминокислоты
Это такие аминокислоты, строение и функции которых вырабатываются в организме:
- аргинин;
- аланин;
- аспарагин;
- глицин;
- пролин;
- таурин;
- тирозин;
- глутамат;
- серин;
- глутамин;
- орнитин;
- цистеин;
- карнитин.
Функции аминокислот заменимых
- Цистеин ликвидирует токсические вещества, участвует в создании тканей кожи и мышц, представляет собой естественный антиоксидант.
- Тирозин снижает физическую усталость, ускоряет метаболизм, ликвидирует стресс и депрессию.
- Аланин служит для роста мускулатуры, является источником энергии.
- увеличивает метаболизм и снижает образование аммиака при больших нагрузках.
- Цистин устраняет боль при травмировании связок и суставов.
- отвечает за мозговую активность, во время длительных физических нагрузок переходит в глюкозу, вырабатывая энергию.
- Глутамин восстанавливает мышцы, повышает иммунитет, ускоряет метаболизм, усиливает работу мозга и создает гормон роста.
- Глицин необходим для работы мышц, расщепления жира, стабилизации артериального давления и сахара в крови.
- Карнитин перемещает жировые кислоты в клетки, где совершается их расщепление с выделением энергии, в результате чего сжигается лишний жир и генерируется энергия.
- Орнитин производит гормон роста, участвует в процессе мочеобразования, расщепляет жирные кислоты, помогает выработке инсулина.
- Пролин обеспечивает производство коллагена, он необходим для связок и суставов.
- Серин повышает иммунитет и вырабатывает энергию, нужен для быстрого метаболизма жирных кислот и роста мышц.
- Таурин расщепляет жир, поднимает сопротивляемость организма, синтезирует желчные соли.
Белок и его свойства
Белки, или протеины - высокомолекулярные соединения с содержанием азота. Понятие "протеин", впервые обозначенное Берцелиусом в 1838 г., происходит от греческого слова и означает "первичный", что отображает лидирующее значение протеинов в природе. Разновидность белков дает возможность для существования огромного количества живых существ: от бактерий до человеческого организма. Их существенно больше, чем других макромолекул, ведь белки - это фундамент живой клетки. Составляют приблизительно 20% от массы человеческого тела, больше 50% сухой массы клетки. Такое количество разнообразных белков объясняется свойствами двадцати различных аминокислот, которые взаимодействуют друг с другом и создают полимерные молекулы.

Выдающееся свойство белков - способность к самостоятельному созданию определенной, свойственной конкретному белку пространственной структуры. По белки - это биополимеры с пептидными связями. Для химического состава белков свойственно постоянное среднее содержание азота - приблизительно 16%.
Жизнь, а также рост и развитие организма невозможны без функции белковых аминокислот строить новые клетки. Белки нельзя заменить прочими элементами, их роль в человеческом организме является чрезвычайно важной.
Функции белков
Необходимость белков заключается в таких функциях:
- он необходим для роста и развития, так как выступает главным строительным материалом для создания новых клеток;
- управляет метаболизмом, во время которого освобождается энергия. После принятия пищи скорость метаболизма увеличивается, например, если еда состоит из углеводов, метаболизм ускоряется на 4%, если из белков - на 30%;
- регулируют в организме, благодаря своей гидрофильности - способности притягивать воду;
- усиливают работу иммунной системы, синтезируя антитела, которые защищают от инфекции и ликвидируют угрозу заболевания.

Продукты - источники белков
Мышцы и скелет человека состоят из живых тканей, которые на протяжении жизни не только функционируют, но и обновляются. Восстанавливаются после повреждений, сохраняют свою силу и прочность. Для этого им требуются вполне определенные питательные вещества. Пища обеспечивает организм энергией, необходимой для всех процессов, включая работу мышц, рост и восстановление тканей. А белок в организме используется и как источник энергии, и как стройматериал.

Поэтому очень важно соблюдать его ежедневное использование в пищу. Богатые белком продукты: курица, индейка, постная ветчина, свинина, говядина, рыба, креветки, фасоль, чечевица, бекон, яйца, орех. Все эти продукты обеспечивают организм белком и дают энергию, необходимую для жизни.
Химические свойства а-аминокислот определяются, в самом общем случае, наличием у одного и того же атома углерода карбоксильной и аминной групп. Специфика боковых функциональных групп аминокислот определяет различия в их реакционной способности и индивидуальности каждой аминокислоты. Свойства боковых функциональных групп выходят на первый план в молекулах полипептидов и белков, т.е. после того, как аминная и карбоксильная группа свое дело сделали - образовали полиамидную цепочку.
Итак, химические свойства собственно аминокислотного фрагмента подразделяются на реакции аминов, реакции карбоновых кислот и свойства, обязанные взаимному их влиянию.
Карбоксильная группа проявляет себя в реакциях со щелочами - образуя карбоксилаты, со спиртами - образуя сложные эфиры, с аммиаком и аминами - образуя амиды кислот, а-аминокислоты достаточно легко декарбоксилируются при нагревании и при действии ферментов (схема 4.2.1).
Эта реакция имеет важное физиологическое значение, поскольку ее реализация in vivo приводит к образованию соответствующих биогенных аминов, выполняющих ряд специфических функций в живых организмах. При декарбоксилировании гистидина образуется гистамин, обладающий гормональным действием. В организме человека он находится в связанном виде, освобождается при воспалительных и аллергических реакциях, анафилактическом шоке, вызывает расширение капилляров, сокращение гладкой мускулатуры, резко повышает секрецию соляной кислоты в желудке.
Так же, реакцией декарбоксилирования, вместе с реакцией гидроксилирования ароматического цикла, из триптофана образуется другой биогенный амин - серотонин. Он содержится у человека в клетках кишечника в тромбоцитах, в ядах кишечнополостных, моллюсков, членистоногих и земноводных, встречается в растениях (бананах, кофе, облепихе). Серотонин выполняет медиаторные функции в центральной и периферической нервной системах, влияет на тонус кровеносных сосудов, повышает стойкость капилляров, увеличивает количество тромбоцитов в крови (схема 4.2.2).
Аминогруппа аминокислот проявляет себя в реакциях с кислотами, образуя аммонийные соли, ацилируется
Схема 4.2.1
Схема 4.2.2

и алкилируется при взаимодействии с галогенангидридами и галогеналкилами, с альдегидами образует основания Шиффа, а с азотистой кислотой, как и обычные первичные амины, образует соответствующие гидроксипроизводные, в данном случае оксикислоты (схема 4.2.3).
Схема 4.2.3

Одновременное участие аминогруппы и карбоксильной функции в химических реакциях достаточно разнообразно. а-Аминокислоты образуют комплексы с ионами многих двухвалентных металлов - эти комплексы построены с участием двух молекул аминокислот на один ион металла, при этом металл образует с лигандами связи двух типов: карбоксильная группа дает с металлом ионную связь, а аминогруппа участвует своей неподеленной электронной парой, координирующейся на свободные орбитали металла (донорно-акцепторная связь), давая так называемые хелатные комплексы (схема 4.2.4, металлы расположены в ряд по устойчивости комплексов).
Так как в молекуле аминокислоты присутствует одновременно и кислотная и основная функция, то безусловно взаимодействие между ними неминуемо - оно приводит к образованию внутренней соли (цвиттер-иона). Так как это соль слабой кислоты и слабого основания, то в водном растворе она будет легко гидролизоваться, т.е. система равновесная. В кристаллическом состоянии аминокислоты имеют чисто цвиттер-ионную структуру, отсюда высокие этих веществ (схема 4.2.5).
Схема 4.2.4

Схема 4.2.5

Нингидринная реакция имеет большое значение для обнаружения аминокислот при их качественном и количественном анализе. Большинство аминокислот реагирует с нингидрином, выделяя соответствующий альдегид, при этом раствор окрашивается в интенсивный сине-фиолетовый цвет ( нм), растворы оранжевого цвета ( нм) дают только пролин и оксипролин. Схема реакции достаточно сложна и ее промежуточные стадии не совсем ясны, окрашенный продукт реакции носит название “фиолетовый Руэмана" (схема 4.2.6).
Дикетопиперазины образуются при нагревании свободных аминокислот, а лучше при нагревании их эфиров.
Схема 4.2.6

Продукт реакции можно определить по структуре - как производное гетероцикла пиразина, по схеме реакции - как циклический двойной амид, поскольку образуется он взаимодействием аминогрупп с карбоксильными функциями по схеме нуклеофильного замещения (схема 4.2.7).
Образование полиамидов а-аминокислот является разновидностью вышеописанной реакции образования дикепиперазинов, причем той
Схема 4.2.7

Схема 4.2.8

разновидностью, ради которой наверное Природа и создала этот класс соединений. Суть реакции заключается в нуклеофильной атаке аминной группы одной а-аминокислоты по карбоксильной группе второй а-аминокислоты, тогда как аминная группа второй аминокислоты последовательно атакует карбоксильную группу третьей аминокислоты и т.д. (схема 4.2.8).
Результатом реакции является полиамид или (называемый применительно к химии белков и белковоподобных соединений) полипептид. Соответственно фрагмент -CO-NH- называют пептидным звеном или пептидной связью.










